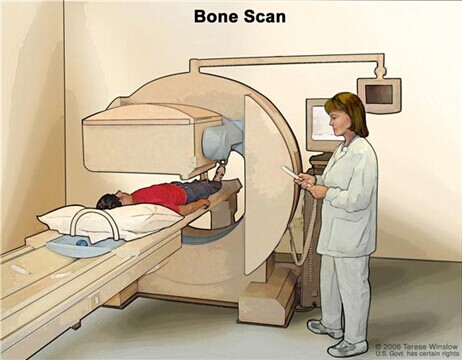
局限性前列腺癌的微創治療進展
羅小美①② 綜述 陳繼冰②③ 牛立志②③ [1] 審校
(① 暨南大學醫學院,廣州,510632;②廣州復大腫瘤醫院,510665;③廣州復大腫瘤醫院,510665)
前列腺癌已成為世界男性最常見的癌癥之一。2013年美國新增前列腺癌患者238590例,因前列腺癌而死亡人數達29720例,是男性僅次于肺和支氣管疾病的第二大死因[1]。前列腺根治術、放射治療、近距離照射、冷凍治療是局限性前列腺癌的主要治療方式。目前很大一部分相對年輕、低危的前列腺癌患者由于潛在的治療并發癥等原因不愿意接受手術、放療等根治性治療;另外,部分患者由于全身情況較差且合并多種內科疾病,無法耐受麻醉與手術;因此,對患者創傷小、療效佳的微創治療方式成為新的需求。近年隨著相關技術的發展,近距離照射、冷凍消融、高能聚焦超聲、光動力治療、納米刀等以其有效、微創、安全的優勢在治療前列腺癌方面發揮著越來越大的作用。本文主要就以上幾種微創治療方法展開論述。
1 主要治療
1.1 近距離照射治療
前列腺癌近距離照射包括短暫插植治療和永久粒子種植治療,后者更為常用,即通過三維系統的準確定位后,將放射源密封后直接放入前列腺內種植治療。與前者相比提高了前列腺的局部劑量,減少直腸和膀胱的放射劑量[2] 。根據美國近距離放射治療學會的標準,單純近距離照射治療前列腺癌的適應癥為:①臨床分期為T1-T2a期;②Gleason評分<6;③PSA<10ng/ml。前列腺體積較大時,可輔以內分泌治療縮小體積。此外,近距離照射還適合于不能耐受前列腺癌根治術的高齡前列腺癌患者。
上世紀80年代,Holm首次將I粒子經會陰前列腺穿刺植入治療前列腺癌[3]。隨后近距離照射治療技術發展迅速。2011年Sylvester等報導對215例局限性前列腺癌患者行單純125I粒子植入治療,隨訪15年,無病生存率為80.4%[4]。2012年Georgakopoulos等研究表明,根治性前列腺切除術、外放射治療、放射性粒子植入治療三種治療方法中放射性粒子植入在提高生活質量方面的優勢尤為突出[5]。2015年Martinez等報導對700例前列腺癌患者行125I放射性粒子近距離植入,5、10年總生存率分別為94%、84%;生化無復發生存率為95%、85%。該報告進一步證實了粒子近距離放射治療前列腺癌長期療效好[6]。
膀胱與直腸是前列腺毗鄰的器官,I粒子的植入在殺傷腫瘤的同時,亦不可避免引起膀胱與直腸黏膜損傷,引起相關尿道癥狀和直腸并發癥。泌尿生殖毒性是近距離照射治療后最常見的毒性反應,但嚴重不良反應少見[7]。2012年丁海雍等報導125I放射性粒子植入治療前列腺癌常見并發癥是尿路刺激癥狀和血尿,而前列腺癌根治術治療前列腺癌常見尿失禁和血尿,個別伴有肺部感染[8]。2015年Zuber等報導對169例早期前列腺癌患者行125I放射性粒子植入治療,治療后5年生化失敗率為7%;急性直腸炎發生率20%,尿失禁發生率約35%[9]。準確的植入技術可以最大限度地減少直腸前壁輻射劑量和近距離放射治療相關的腸道發病率。
前列腺癌近距離治療的優點:適應證與前列腺癌根治術一樣;無絕對的年齡限制;創傷小,相對禁忌證少;不需考慮陽痿及尿失禁的發生;療效可靠,易被患者接受;新輔助內分泌治療后,T2c期和部分T3期患者仍可進行治療。但放射
性粒子的毒性作用使其前列腺癌治療中應用受限。總體來說,前列腺癌近距離照射是繼前列腺癌根治術及外放療外的又一種有望根治局限性前列腺癌的方法。
1.2 冷凍消融
冷凍消融通過冷凍細胞至-40℃可將前列腺癌組織殺死,并引發組織的凋亡和炎性反應瀑布殺傷腫瘤。根據手術徑路可分為經尿道冷凍術、經腹冷凍術和經會陰穿刺冷凍術。最常用的是經會陰穿刺冷凍術。目前學術界還沒有對前列腺癌冷凍治療適應證形成統一觀點。《歐洲泌尿外科學會前列腺癌指南》指出前列腺癌冷凍治療的適應證為:①病灶局限于前列腺內的患者;②病灶輕微突破前列腺的患者;③前列腺體積應該≤40mL(以保證有效的冷凍范圍),如>40 mL的患者應該采用新輔助內分泌治療使腺體縮小;④PSA<20ng/mL;⑤Gleason評分<7。
2010年Donnelly等報導對244例局部前列腺癌患者隨機分配接受冷凍或外放射治療,結果發現兩個治療組在3年總生存率和無病進展率方面均無明顯差別[10]。2012年Bahn等研究報導冷凍治療和前列腺根治術治療單側性前列腺癌療效相似[11]。2012年Chin等研究報導與外放射治療相比,冷凍治療局限性前列腺癌8年生化無進展生存率更低,總生存率相似[12]。2014年屈峰等對17例去勢抵抗性前列腺癌患者行冷凍消融聯合多西紫杉醇化療治療,平均隨訪31月,PSA 無進展生存率為94.1%,疾病緩解的患者的PSA中位進展時間為54.2周,中位生存期>14個月[13]。
近期研究冷凍消融還可以用于挽救性治療,其5年無生化復發生存率達到50%-70%[14]。2013年Wenske等對328例前列腺癌患者行挽救性冷凍治療,其5、10年無病生存率為63%和35%;總生存率為74%和45%[15]。2015年Chang等報導對12例局限性復發前列腺癌患者采取冷凍治療,治療前后中位PSA值為2.5 ng/ml vs 1.32 ng/ml;隨訪33.5個月,其中1例出現輕度尿失禁,1例出現尿道脫落,2例出現一過性陽痿[16]。
冷凍治療前列腺癌可引起性功能降低[17]。勃起功能障礙是前列腺癌冷凍治療最主要的并發癥,有研究報導采用第三代冷凍系統,術后勃起障礙的發生率在87%~88%之間[18]。隨著冷凍技術的改進,直腸尿道瘺形成的發生率下降。其它的并發癥有組織脫落、尿失禁、尿儲留等。2014年Marien等報導冷凍治療與高能聚焦超聲相比副反應發生率較少,但反應較嚴重,約15%-40%出現勃起功能障礙,尿失禁發生率約1%-10%;約60%-94%前列腺癌患者經冷凍治療后活檢無復發[19]。
與其他局部治療方式相比,冷凍在前列腺癌治療中體現了顯著的臨床療效。冷凍消融可以實時監測冷凍溫度,控制冷凍冰球大小,控制壞死區域;根據個體情況可單根或多根探針同時使用,可重復治療。但冷凍消融可引起性功能較低,不適用于對性功能要求較高的患者;術中不能燒灼探針經過的孔道,增加了出血、腫瘤播散的風險,且治療時間延長、成本較高。隨著冷凍設備的改進和技術的提高,冷凍治療局限性前列腺癌越來越受大眾青睞,應用前景廣闊。
2 試驗性局部治療
2.1 高能聚焦超聲(High—intensity focused ultrasound,HIFU)
HIFU是通過體外發射高能超聲波,在體內將超聲波能量聚焦在選定的臟器組織區域內,使溫度高于65℃使腫瘤組織發生凝固性壞死。自1996年Gelet等首次使用HIFU治療前列腺癌[20]起,HIFU開始逐漸應用于治療前列腺癌。HIFU適用于低危及中危局限性前列腺癌患者。目前HIFU治療能在門診完成,已被申請作為局限性前列腺癌的一線治療,也可作為放療失敗患者的挽救性療法。
許多研究已證實HIFU對局限前列腺癌有較好的控制率。2012年Sung等報導對157例前列腺癌患者行HIFU治療,總體生化復發率為59.5%,中位生化復發時間為13.8個月;低危、中危和高危組5年生化無復發生存率分別為66.3%、40.2%和21.0% [21]。2013年Ganzer等報導應用HIFU治療538例局限性前列腺癌,治療后19.9周患者平均PSA值為0.4μg/L;低危、中危和高危組遠處轉移的發生率分別為0.4%、5.7% 和15.4%[22]。2015年Uchida等報導對918例前列腺癌患者行HIFU治療, 5年總體活檢陰性率為87.3%;10年總體生存率和癌癥特異性生存率分別為89.6%和97.4%;其中相關并發癥尿道狹窄、附睪炎、尿失禁和尿道直腸瘺發生率分別為19.7%、6.2%、2.3%和0.1%[23]。近年研究認為HIFU也可用于挽救治療。2012年Asimakopoulos等對19例前列腺癌根治術后局部復發的患者行HIFU治療,治療后17例患者血清PSA值≤0.1 ng/mL,隨訪48個月,生化復發失敗率為52.6%[24]。HIFU在控制腫瘤發展方面效果較好,副作用小,與根治術相比嚴重并發癥較少[25]。
HIFU在消融過程中可同時成像,消融范圍精確,并發癥少、無劑量限制、可重復治療;聯合內分泌治療、放療或化療等進行綜合性治療,可改善高風險前列腺癌或晚期腫瘤的治療效果。但HIFU作為一項新技術,在臨床應用中仍存在一些問題。如在治療時不能進行無創性實時測溫,導致治療過程中無法明確靶區的治療溫度,不能完全殺死腫瘤細胞,而造成靶區內癌細胞殘留,引起腫瘤復發。此外,HIFU在前列腺癌的治療方面尚無公認的治療規范和療效判斷標準,在臨床研究方面還缺少劑量與療效的關系、大樣本隨機對照研究和遠期臨床療效觀察。
2.2 血管靶向光動力治療(Vascular-targeted photodynamic therapy,VTP)
VTP作為治療治療局限性前列腺癌的一種手段越來越多地受到關注。VTP是指將光敏劑經靜脈導入,然后通過局部激光照射活化誘導腫瘤壞死。目前正在研究中的光敏劑Tookad(WST09)及其水溶衍生物WST11[26]。
2013年Barret 等對23例局限性前列腺癌患者采取VTP治療,治療前中位PSA為6.1 ng/ml,治療后3、6、12月中位PSA為3.1、2.9、2.7 ng/ml,無嚴重并發癥發生[27]。
VTP對腫瘤細胞具有相對選擇性和組織特異性,但由于激光照射深度不足,照射強度不均勻,引起的細胞壞死也不一致,因此VTP治療前列腺癌仍在試驗階段。
2.3 射頻消融(Radiofrequency ablation,RFA)
RFA是把電能充分地轉化為熱能,通過提升靶組織的溫度,產生凝固性壞死,以實現對病灶的滅活;由于高溫啟動機體特異性T淋巴細胞,引起繼發性抗腫瘤免疫,有利于機體清除腫瘤細胞。
2006年Patriar等研究表明,組織內腫瘤射頻消融治療前列腺癌5分鐘可使腫瘤組織產生凝固性壞死,該作者認為組織內腫瘤射頻消融治療是安全有效,可重復,可控制的[28]。2013年林新等對30例前列腺癌患者在CT的引導下行多極射頻消融術進行治療,結果示顯效53.3%、有效26.7%、穩定20.0%,治療后有發熱、血尿、局部血腫與尿路刺激的情況發生,經對癥治療后均得到緩解。
目前前列腺癌RFA臨床應用進展較慢,可能與前列腺特殊的解剖位置、并發癥較大有關系,此外,射頻在高阻抗的組織中蓄積能量存在難度,影像學不清晰,易引起腫瘤殘留,周圍組織損傷。目前RFA治療前列腺癌的報導相對較少,僅有小樣本的I/11期臨床試驗探討了RFA治療前列腺癌的可行性和安全性。其遠期臨床療效還需大樣本的長期隨訪研究證實。
2.4 微波熱療
前列腺微波熱療是通過加熱前列腺腫瘤組織到55~7O℃,使腫瘤細胞殺死,同時保護前列腺周圍主要的組織,如直腸、膀胱、尿道。自從2O世紀80年代起,微波熱療在很多國家被用于腫瘤治療。
早前Sherar等報導采用微波熱療治療25例局限性前列腺癌復發患者,治療過程安全且無明顯并發癥[29]。曾報導的并發癥有膀胱痙攣、出血、尿道損傷、感染等。Shera等報導在微波熱療后,沒有出現嚴重的并發癥。微波熱療不會引起逆向射精,并且可以將治療后勃起障礙的風險最小化[30]。
微波熱療治療前列腺癌報導較少,暫不能對其安全性和有效性作出評價,仍有待進一步臨床研究。
2.5 納米刀
納米刀也稱不可逆電穿孔(Irreversible Electroporation,IRE),是通過電極探針釋放微秒級的高壓脈沖擊穿腫瘤細胞的細胞膜上形成納米級不可逆的微穿孔,造成腫瘤細胞凋亡瓦解,凋亡后的腫瘤所在區域逐漸被正常組織取代,從而恢復正常機能。納米刀已經率先在美國得到FDA批準應用于臨床取得良好效果,歐洲也開始使用,近來香港中文大學醫院,臺大醫院都分別開展了地區首例納米消融治療肝腫瘤的臨床應用。
2011年Brausi等首次報導在11例低風險前列腺癌患者中行IRE試驗安全性研究,治療后無嚴重并發癥發生,急性尿潴留1例,一過性尿失禁3例;治療后1、3、6、19個月平均PSA值分別為3.5、2.9、3.3和3.12 ng/mL;前列腺活檢陰性8例[31]。2014年Valerio等報導對34例前列腺癌患者行IRE,術后95%的患者保留了性功能,沒有三級及以上并發癥發生,證實IRE治療前列腺癌有助于提高泌尿生殖功能,毒性低[32]。同年Van den Bos等報導IRE消融治療前列腺癌安全有效,IRE可以有效地殺死腫瘤細胞和保護周圍組織和重要結構[33]。納米刀依賴電能消融組織,可誘發動作電位,導致肌張力增高及心律失常等,因此需在全身麻醉狀態下配備心臟同步器進行治療。
相比射頻消融及冷凍消融治療腫瘤,IRE有如下優點:①治療時間短,3公分腫瘤納米消融不超過5分鐘。②IRE不依賴溫度變化,治療區域的重要組織不會受到誤傷。③治療徹底,治療區域清晰,全程可以實時監控。④治療區域的組織可以在短時間內被正常細胞替代從而恢復正常組織功能[34]。IRE相比射頻消融及冷凍消融,在靠近肝門腫瘤,胰腺腫瘤,貼近腸道尿道及膀胱的腫瘤方面有獨特優勢。
3 小結
經過多年的發展,前列腺近距離照射、冷凍消融等治療技術已較為成熟,應用較廣,但各有優缺點,并發癥不同,適合不同需求的患者。高能聚焦超聲、血管光動力、納米刀等治療前列腺癌目前研究結果令人欣喜,但仍需大量的臨床研究進一步發展完善。射頻、微波在前列腺癌研究發展較慢,應用受限。隨著相關技術及設備的不斷發展,前列腺癌的微創治療有著廣闊的發展前景,但仍還存在著較多問題亟待解決。單純微創治療療效是有限的,聯合內分泌治療、放療或化療等綜合治療有望提高局限性前列腺癌的治療效果。
參考文獻
略
廣州復大腫瘤醫院“3C+P”治療模式智能抗前列腺癌
牛立志智慧抗癌 實現菲律賓將軍愛情健康雙豐收
2015年3月15日,廣州復大腫瘤醫院院長牛立志博士因應邀出席菲律賓會議,這也許就是緣分,在途中竟偶遇他之前醫治過的病人和他太太。這位病人不是一般人,而是菲律賓的一位將軍。牛立志博士和他們短聚,看著眼前容光煥發的兩人,深深地為他們這段佳偶天成祝福...
兩年前,菲律賓將軍來復大腫瘤醫院的決心與理由
兩年前,將軍很不幸地患上前列腺癌,情況已經非常嚴重,四處求醫但沒有醫院能夠收治他。經過多方打聽到中國廣州的復大腫瘤醫院,他了解到復大腫瘤醫院一些相關信息:第一,“3C+P”治療模式可使70%左右中晚期癌癥,包括已做常規治療而無效,或復發的患者,得以改善或長期生存,有的近乎“治愈”;第二,復大腫瘤醫院以“真實的技術”和“真誠的服務”,吸引了國內外癌癥患者;全世界76個國家的患者前來就診,住院病人70%以上來自東南亞、中東、西歐、北美等地區。他看中了這兩點,不畏千辛萬苦地找到復大腫瘤醫院,希望為自己治療。
“3C+P”治療模式讓將軍成功抗擊前列腺癌
萬分驚訝下,復大腫瘤醫院總院長徐克成教授和牛立志博士即刻為將軍商討治療方案,在牛立志領導的醫學團隊下,采用“3C+P”治療模式為其治療。針對性強及個體化的治療方案,讓將軍的病人很快得到控制。出院之際將軍不停地盛贊復大腫瘤醫院是他第二次生命的始源地,同時也非常感謝復大腫瘤醫院杰出的專家團隊。他盛情邀請徐克成教授以及牛立志博士來菲律賓做客。
牛立志博士談到這次與將軍見面情景,他說,“和將軍他們相談甚歡,將軍他已經80多歲了,一時間我竟認不出他來,顯得比之前越發年輕了,容光煥發,更值得高興的是,將軍所有的身體檢查均顯示正常!將軍恢復得這么神速,還真多虧他身邊有位細心、慈愛、善良的紅顏知己。”
在這兩年的時間里面,將軍愛情健康雙豐收,將軍說道,“活到這把年紀,健康有了,愛情也有了,人生沒有遺憾了。這一切真是多虧復大腫瘤醫院和牛立志博士你啊。要不是你們的醫術醫德,很有可能就已經早走了,非常感激你們...”

牛立志博士在會議上偶遇菲律賓將軍夫婦
廣州復大腫瘤醫院“3C+P”治療模式治療效果
近十年來,復大腫瘤醫院采用國際最新抗癌理念,將世界醫學難題——中晚期惡性腫瘤作為主要治療對象,以延長患者壽命、改善患者生活質量作為主要目標,重點開展以氬氦冷凍消融治療(CSA)、微血管介入療法(CMI)、聯合免疫療法(CIC)和個體化應用(P)為復大腫瘤醫院主導的“3C+P”治療模式。其中氬氦冷凍消融治療腫瘤方面上,例數字列世界第一;在治療中央型肺癌、巨大肝癌和胰腺癌方面,廣州復大腫瘤醫院有著突出的成就,多次獲國內外大獎。
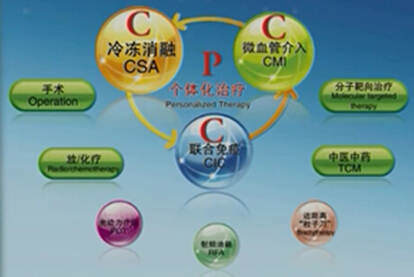
復大腫瘤醫院倡導的“3C+P”治療模式