一、概述
成人原發性肝癌是一種源于肝組織的惡性細胞癌。
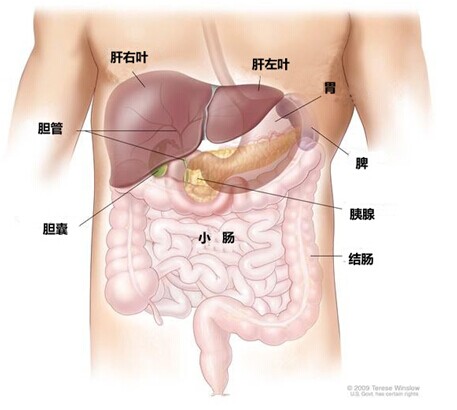
肝臟是人體最大的腺體,最重要的消化器官、代謝器官和防御器官,是人體新陳代謝的樞紐。自下腔靜脈左緣至膽囊窩中點的正中裂將肝臟分為左半肝和右半肝,包括左內葉、左外葉、右前葉和右后葉四部分。其主要功能包括三方面:
l 解毒:過濾血液中的有害物質,使之隨糞便和尿液排出體外。
l 分泌和排泄膽汁:分泌和排泄膽汁,以促進脂肪在小腸內的消化和吸收。
l 糖原儲存:儲存的糖原(糖),為機體活動提供能量。
成人原發性肝癌有兩種類型
• 肝細胞癌
• 膽管癌
其中最常見的類型是肝細胞癌。
原發性肝癌可發生于成人和兒童。然而,兒童肝癌的治療與成人有所不同。
二、原發性肝癌的危險因素
肝炎或肝硬化可增加成人原發性肝癌的患病風險。
l 病毒性肝炎:乙型肝炎和丙型肝炎可顯著增加肝癌的患病風險。
l 家族史:直系親屬中有肝炎和肝癌患者。
l 肝硬化,它可以由以下原因引起:
- 肝炎(尤其是丙型肝炎)
- 長期大量飲酒
- 黃曲霉素:食用被黃曲霉素污染的食物(存儲不當的谷物和堅果等食物常含有些類真菌)。
- 血色病:此類患者的機體會吸收比正常人更多的鐵,多余的鐵被存儲在肝臟、心臟和胰腺。
三、原發性肝癌的癥狀
原發性肝癌主要癥狀是右腹部腫塊或疼痛,如有以下癥狀請咨詢您的醫生:
l 右側肋骨后可觸摸到硬疙瘩
l 右上腹部不適感
l 腹部腫脹
l 右側肩胛骨或背部疼痛
l 黃疸(皮膚和眼白變黃)
l 容易瘀傷或出血
l 經常感到疲倦
l 惡心、嘔吐。
l 食欲不振。
l 不明原因的體重下降。
以上癥狀可由原發性肝癌或其它疾病引起,具體原因請與您的醫生詳細溝通。
四、原發性肝癌的檢測與診斷:
檢測和診斷本病的主要手段包括肝臟檢查和血液檢測,包括:
l 體檢和病史:全身性體檢,包括檢查是否有腫塊或其他任何疾病的征兆。調查您的過往健康情況、疾病情況和治療情況。
l 血清腫瘤標記物檢測:甲胎蛋白(AFP)在血液中水平的增加對肝癌具有診斷價值。其他癌癥和某些非癌性條件,包括肝硬化和肝炎,也可能會增加AFP水平。但也有些肝癌患者的AFP水平處于正常狀態。
l 肝功能檢查:通過血液樣本檢測肝臟釋放到血液的的各物質的量。高于正常值的指標可能是肝癌的指征。
l CT掃描(CAT掃描):是通過連接到的X射線機的計算機對機體某個部位進行一系列掃描和拍攝的檢查。檢查前,將需要您吞食或通過靜脈注入一種造影劑,幫助器官或組織顯示得更加清晰。
l MRI(磁共振成像):是使用一個磁鐵、無線電波和計算機,對機體某個部位進行細致掃描和拍攝的檢查,這個過程也被稱為核磁共振成像(NMRI)。為使肝臟周圍血管更清晰地顯影,可通過靜脈注入造影劑,這個過程被稱為MRA(磁共振血管造影)。
l 超聲檢查:通過高能量聲波(超聲波)探測組織或器官的情況。
l 活檢:從腫塊上切取一些細胞或組織,由病理學家在顯微鏡下檢查癌癥的跡象。此項并非成人原發性肝癌的必要檢查。
五、影響原發性肝癌預后以及治療方案的因素
l 癌癥的分期(腫瘤的大小,以及是否已經擴散到身體其它部位)。
l 肝功能情況 。
l 患者的一般健康狀況,包括是否有肝硬化等。
六、原發性肝癌分期
在診斷后,應了解腫瘤范圍和擴展情況,以確定分期。CT掃描(CAT掃描)、MRI(磁共振成像)、PET-CT等檢查有助于分期,以了解腫瘤位置、大小、與周圍器官關系、有無遠處器官轉移等。
巴塞羅納臨床肝癌分期系統(The Barcelona Clinic Liver Cancer Staging System,BCLC Staging System)被廣泛應用,可指導評估疾病的預后和治療方案的制定。它將肝癌分為5期:
0期:極早期
I期:早期
II期:中期
III期:進展期
IV期:晚期
對于0期、I期和II期病人,有可能可通過治療達到治愈;對于III期和IV期的病人,可通過治療使肝癌的癥狀得到緩解,并提高病人的生存質量。III期和IV期肝癌不可治愈。
成人原發性肝癌有下列3種擴散途徑:
l 組織:直接擴散到臨近組織。
l 淋巴系統:腫瘤通過淋巴系統擴散到身體的其他部位。
l 血液:腫瘤細胞通過進入血液擴散到其他器官。
腫瘤細胞擴散到其他器官,稱為轉移,即腫瘤細胞從原有的腫瘤上脫離出來,并通過淋巴系統或血液轉移到身體的其他部位。
轉移瘤與原發瘤是同一種類型的腫瘤。例如,如果原發性肝癌轉移到了肺,那肺上的癌細胞還是肝癌細胞,稱為轉移性肝癌,而非肺癌。
七、原發性肝癌治療概述
• 手術
部分肝切除術(手術切除肝臟的腫瘤部位)。根據腫瘤大小可能切除肝臟的一小部分、一個肝葉或大半個肝臟,包括腫瘤以及其周圍的一些正常肝組織。剩余的肝組織仍然能發揮肝臟的正常功能,并且可以再生。
• 肝移植
肝移植即是用一個健康的肝臟替換原有的肝臟。這種方法只適用于腫瘤只存在于肝臟而未發生任何轉移,且可以找到捐贈的肝臟。在肝源的等待期需要必要的治療支持。
• 消融治療
消融療法可去除或破壞腫瘤組織。以下類型的消融療法可用于肝癌治療:
• 冷凍消融:即使用冷凍設備來凍結和破壞癌細胞的一種治療方法。這種療法也被稱為冷凍療法或冷凍手術。可通過超聲或/和CT來引導實施經皮冷凍消融,具有定位更精確、消融范圍更精準、創作更微小、安全性更高、副作用更少的特點。
• 射頻消融:將電極針經超聲引導下經皮插入腫瘤,通過高頻交流電作用,將腫瘤回熱至40℃~60℃,使腫瘤細胞凝固、壞死(腫瘤細胞在42.5-43.5℃的溫度下就會萎縮以至于死亡)。
• 微波治療:用微波治療腫瘤的方式有二種,一種是微波從體外照射進去,另一種是把微波送到患部直接照射腫瘤,這二種治療方式可根據病變部位來選擇。微波產生的高溫會損傷和殺死癌細胞或使它們對放療和化療更為敏感。
• 經皮無水酒精注射:在B超或CT引導下利用小針筒直接將無水酒精注入腫瘤中央,使腫瘤細胞及附近血管內皮細胞迅速脫水,蛋白質變性凝固,導致腫瘤細胞壞死/缺血。通常可在局部麻醉下進行,但如果需對肝臟中的多個腫瘤同時操作,可以選擇全身麻醉。
• 電穿孔療法:通過放置在腫瘤中的電極發送的電脈沖,達到殺死癌細胞的效果。
• 栓塞治療
栓塞治療是利用物質阻止或減少通過肝動脈輸送到腫瘤組織的血液。當腫瘤失去氧氣和營養物質的供給,就會停止生長。栓塞治療適用于不能手術切除或消融治療,且沒有肝外轉移的腫瘤。
栓塞療法主要包括兩種類型:
• 經動脈栓塞(TAE):在大腿內側開一個小切口,將一根較細且柔軟的導管插入并上行至肝動脈。一旦導管就位,即注入一種栓塞物質,阻斷肝動脈輸送到腫瘤的血流。
• 經動脈化療栓塞(TACE):治療程序與TAE相似,只是在TAE的基礎上再加入抗腫瘤化療藥。大部分藥物將聚集在腫瘤部位,只有少量的藥物會去到身體的其他部位。此療法也稱為化療栓塞。
• 靶向治療
靶向治療是使用靶向藥物或其他物質,來識別和攻擊特定腫瘤細胞而不傷害正常細胞的一種治療。成人肝癌可以通過靶向藥物治療,停止細胞分裂,并阻止腫瘤新血管的生長。
• 放射治療
放射治療是利用高能量X-射線或其他類型的輻射殺死癌細胞或阻止他們不斷增長的治療方式。放射治療包括以下兩種:
• 體外照射:又稱為遠距離放射治療。在身體外部對腫瘤部位進行射線照射。
• 體內照射:又稱為近距離放射治療。把高強度的微形放射源送入人體腔內或配合手術插入腫瘤組織內,進行近距離照射,從而有效地殺傷腫瘤組織。放射性粒子植入是常見的近距離放射治療,是指在B超或CT引導下,可精確地將放射性粒子均勻地置入腫瘤周圍,通過放射性粒子持續釋放射線來達到最大限度地殺傷腫瘤細胞的作用。
八、我院:肝癌特色治療
l 腫瘤冷凍消融(CSA):應用美國制造的氬氦冷凍系統,在超聲或CT的引導下,將冷凍探針插入腫瘤內,輸入氬氣,探針頂端溫度急劇將至攝氏零下160-170度,將腫瘤細胞凍死,然后換輸氦氣,溫度上升至攝氏40度,使腫瘤溶解。本法適合不能手術切除的腫瘤。應用該法治療各類不可手術切除性肝癌,包括大肝癌、轉移性肝癌等,已取得較好效果,有效地延續病人生命。
l 經皮無水酒精注射:在B超或CT引導下利用小針筒直接將無水酒精注入腫瘤中央,使腫瘤細胞及附近血管內皮細胞迅速脫水,蛋白質變性凝固,導致腫瘤細胞壞死/缺血。通常可在局部麻醉下進行,但如果需對肝臟中的多個腫瘤同時操作,可以選擇全身麻醉。
l 非可逆性電穿孔療法:通過瞬間釋放高壓電流脈沖,引起細胞不可逆性穿孔,達到殺死癌細胞的效果。
l 腫瘤微血管介入治療(CMI):將化療藥物配置成納米形式,通過動脈插管,將納米級藥物輸入腫瘤內。藥物能透過泄漏的腫瘤血管進入腫瘤內,如此用微量藥物可達到最大的抗腫瘤血管。又由于藥物不易透過正常血管,因此不會引起嚴重副作用。本法可使腫瘤縮小,在手術前或后應用。
l 聯合免疫治療(CIC):腫瘤生長和進展與機體免疫功能十分健全有密切關系。良好的免疫功能可遏止腫瘤發展。采用多種免疫調節措施,提高患者免疫功能,至少與腫瘤細胞處于“平衡”態勢,“與瘤共存”,是防止腫瘤復發的重要手段。
我們將上述方法組合起來,按照病人具體情況,制定獨特的個體化微創治療模式,實施全方位治療。
九、相關論著
[1] 徐克成, 牛立志, 何衛兵, 郭子倩, 左建生. 肝癌經皮消融治療. 國外醫學消化系疾病分冊, 2003, 23增:24-27.
[2] 徐克成, 牛立志, 何衛兵, 郭子倩, 左建生. 肝癌經皮消融治療. 現代消化及介入診療, 2003, 8(4):185-192.
[3] 徐克成, 牛立志, 胡以則, 何衛兵, 郭子倩, 左建生. 經皮冷消融聯合酒精注射治療不能切除的肝細胞癌. 中華消化雜志, 2003,23(9):544-547.
[4] 徐克成, 牛立志, 周強, 何衛兵, 郭子倩, 左建生. 化學栓塞一冷消融一酒精注射序貫治療不能手術切除的肝細胞癌. 現代消化及介入診療, 003,8(3):128-142.
[5] 徐克成, 牛立志, 何衛兵, 郭子倩, 左建生, 胡以則. 化學栓塞—經皮冷消融序貫治療不能切除的原發性肝癌. 現代消化及介入診療, 2004, 9(3): 134-137.
[6] 徐克成. 肝癌復發及其預防. 現代消化及介入診療, 2005,10(2):
[7] 郭子倩, 郭德鴻, 牛立志, 何衛兵, 周強, 徐克成. 冷凍一化學消融治療肝臟巨大結節樣增生一例. 中華消化雜志, 2005,25(7):390.
[8] 楊傳標, 郭子倩, 左建生, 牛立志, 徐克成. 不宜手術的中晚期肝癌中醫藥治療方法探析. 新中醫, 2005,37(9).
[9] 徐克成, 牛立志, 周強, 何衛兵, 郭子倩, 左建生. 化學栓塞_冷消融_酒精注射序貫治療不能手術切除性肝細胞癌51例. 中國交通醫學雜志, 2006, 20(2): 136-137.
[10] 楊傳標, 郭德鴻, 左建生, 徐克成, 張曼. 中醫藥治療中晚期肝癌87例臨床觀察. 中國中醫藥科技, 2006,13(6)
[11] 徐克成. 原發性肝細胞癌復發及其預防. 中國交通醫學雜志, 2006,20(1):4-7.
[12] 廖春英, 連曉娜, 鄢細蓮. 肝動脈化學栓塞一氬氦刀冷凍消融一乙醇注射序貫治療晚期肝癌的護理. 中國實用護理雜志, 2007,23(12):37-38.
[13] 楊傳標, 張曼, 王紅, 廖春英, 左建生, 徐克成. 大鼠肝癌濕熱證、脾虛證與野生型p53 mRNA、N-ras 表達相關性研究. 第一軍醫大學學報, 2007,27(11):1738-1742.
[14] 楊傳標, 郭德鴻, 張曼, 左建生, 徐克成. 中醫藥辨證治療中晚期肝癌臨床療效觀察. 南方醫科大學學報, 2007,27(8).
[15] 楊傳標, 張述平, 汪道遠, 袁靖, 左建生, 徐克成. 肝癌中醫證型與野生型p53mRNA、N-ras蛋白表達相關性研究. 新中醫, 2007,39(1).
[16] 冼少雀, 陳偉芳, 廖春英, 王小玲. 經皮靶向氬氦冷消融治療肝癌護理體會. 國際醫藥衛生導報, 2008,14(3): 85-88.
[17] 楊傳標, 周亮, 張長明, 李永強, 左建生, 徐克成. 健脾康復方對大鼠實驗性肝癌IGF-ⅡmRNA表達影響的實驗研究. 中國中醫藥科技, 2008,15(2).
[18] 徐克成,牛立志. 肝癌的冷凍治療. 世界華人消化雜志, 2008,16(3):229-235.
[19] 梁冰, 袁靖,王赫,呂洪軒,牛立志, 楊大明, 徐克成. 擬似肝癌的肝結核2例. 胃腸病學. 2009,14(6):381-383
[20] 楊傳標, 文衛鋒, 孔小峰, 穆峰, 徐克成. 健脾康丸對大鼠實驗性肝癌IGF-ⅡmRNA表達的影響. 中國中醫藥科技, 2009,16(5):347-348.
[21] 周紅桃, 牛立志, 周亮, 穆峰, 張長明, 梁冰, 楊大明, 徐克成. 肝癌患者冷消融后部分生化指標和前炎癥因子的變化. 胃腸病學和肝病學雜志, 2009,18(2):110-112.
[22] 徐克成, 楊大明. 射頻治療原發性肝癌. 胃腸病學和肝病學雜志, 2009,18(4):305-307.
[23] 梁冰, 王赫, 楊大明,徐克成. 臨床病例討論:腹脹、右上腹疼痛、肝內占位性病變. 胃腸病學和肝病學, 2009,18(9):831-33
[24] 王赫, 梁冰, 袁靖, 呂洪軒, 楊大明,牛立志,徐克成. 原發性肝淋巴瘤一例并文獻復習. 中華消化雜志, 2009,29(2):134-135.
[25] 牛立志, 王靜, 周亮, 吳炳輝, 穆峰, 李海波, 胡勇, 胡以則, 左建生, 徐克成. 冷凍治療320例肝癌的并發癥分析及處理. 中國腫瘤臨床與康復. 2010,11(6):508-510.
[26] 牛立志, 徐克強, 梁冰, 王峰, 周亮, 左建生, 徐克成. 肝轉移瘤冷凍治療后“冷休克”3 例報告. 現代消化及介入診療, 2010,15(2):122-124.
[27] 徐克成, 牛立志, 周強, 胡以則, 郭德鴻, 劉正平, 梁冰, 穆峰, 李鷹飛, 左建生. 經動脈化學栓塞和經皮冷凍序貫治療肝細胞癌. 中華消化雜志, 2010,30(10): 745-749.
[28] 陸天雨, 楊大明, 左建生, 徐克成. 小分子靶向藥物治療肝細胞癌的研究進展. 國際消化病雜志, 2011,31(4):219238.
[29] 王峰, 梁冰, 牛立志, 左建生, 邱大衛, 楊大明, 徐克成. 貝伐單抗聯合5-氟尿嘧啶治療進展期胃癌伴多發性肝轉移1例. 胃腸病學, 2010,15(11):702-703.
[30] 姚飛,曾健瀅,陳繼冰,周亮,劉衛群,吳炳輝,方剛,鄧春娟,陳志賢,冷尹,鄧敏,張波,鄧春梅,李家亮,何麗華,牛立志,左建生,徐克成. 不同循環冷凍消融術對西藏小型豬肝部冷凍消融效果的比較. 中華肝膽外科雜志, 2012,18(11):867870.
[31] 武興杰,周強,鄧軍,黃樹圭. 肝癌動脈化療栓塞后殘留病灶的介入治療. 中華全科醫學, 2012,10(8):12101212.
[32] Jialiang Li, Jibing Chen2, Liang Zhou1, Jianying Zeng1, Fei Yao1, Binghui Wu1, Gang Fang, Chunjuan Deng, Zhixian Chen, Yin Leng, Keqiang Xu, Lizhi Niu, Jiansheng Zuo, Kecheng Xu. Comparison of Dual and TripleFreeze Protocols for Hepatic Cryoablation in a Tibet Pig. Model cryobiology, 2012,64:245249.
[33] Feng Mu, Lizhi Niu, Haibo Li, Mengtian Liao, Li Li, Chunyan Liu, Jibing Chen,Jialiang Li, Jiansheng Zuo, Kecheng Xu. Percutaneous comprehensive cryoablation for metastatic hepatocellular cancer. Cryobiology. 2012 Dec 10.
[34] Xu Kecheng, Niu Lizhi, He WB, Guo ZQ, Hu YZ, Zuo Jiansheng. Combination of percutaneous cryoablation with transarterial chemoembolization for treatment of hepatocellular carcinoma.. W J G, 2003 ,9(12):2686-9.
[35] KeCheng Xu, LiZhi Niu, WeiBin He, ZiQian Guo, Yi-Ze Hu, JianSheng Zuo. Percutaneous cryoablation in combination with ethanol injection for unresectable hepatocellular carcinoma. Modern digestion and intervention, 2003,9(12): 2686-2689.
[36] Kecheng Xu, Lizhi Jiu, Weibing He, Yizi Hu, Jiansheng Zuo. Percutaneous cryosurgery for the treatment of hepatic colorectal metastases. W J G, 2008,14(9):1430-1436.
[37] KeCheng Xu, LiZhi Niu, Qiang Zhou, Yi-Ze Hu, De-Hong Guo, ZhengPing Liu, Bing Lan, Feng Mu, Ying-Fei Li, JianSheng Zuo. Sequential use of transarterial chemoembolization and percutaneous cryosurgery for hepatocellular carcinoma. W J G, 2009,15(29):3664- 3669.
[38] LiZhi Niu, Feng Mu, JianYing Zeng, MengTian Liao, Fei Yao, Li Li, ChunYan Liu, JiBing Chen, JiaLiang Li, JianSheng Zuo, KeCheng Xu. Combination treatment with comprehensive cryoablation and immunotherapy in metastatic hepatocellular cancer. WJG , 2013.22(19):1-8.
[39] Juanjuan Shi , Lizhi Niu, Zhifeng Huang, Feng Mu, Jibing Chen, Jialiang Li, Kecheng Xu. Diagnosis and treatment of coagulopathy following percutaneous cryoablation of liver tumors: Experience in 372 patients. Cryobiology, 2013,67:146-150.
[40] Long Xin’an, Zeng Jianying, Niu Lizhi, Yao Fei, Wang Xiaohua, Chen Jibing, Li Jialiang,Xu Kecheng. Alleviating the pain of unresectable hepatic tumors by percutaneous cryoablation: Experience in 73 patients. cryobiology, 2013,67:369-373.
[41] 牛立志,李家亮,曾健瀅,徐克成. 氬氦刀冷凍肝癌的研究進展. 廣東醫學, 2013.34.增刊.
十、專家建議
如果你或你的親友需要作肝癌治療,建議你找以下專家咨詢:
吳孟超-徐克成肝癌中心
徐克成教授
牛立志博士
李朝龍教授
楊大明教授
畢向軍博士
樸相浩博士
十一、治療成功病例故事
十二、相關媒體報道
徐克成著:《我對癌癥患者講實話》廣州:廣州出版社. 2010:25-41
十三、相關視頻
《科技之光—凍結癌細胞》
十四、預防和康復
對于已獲得有效治療的癌癥患者,最重要的是預防復發,延續生命。轉移是復發的主要形式。預防轉移如同預防癌發生那樣,但與患者能否生存下來有更直接關系。
預防復發的策略應該是讓癌癥成為“慢性病”,像高血壓、糖尿病那樣,長期控制,讓癌細胞盡可能長的“休眠”,與人體“和平共處”。
癌細胞是不可能“斬盡殺絕”的,原因有二:(1)癌癥轉移是“早期事件”,即使“早期”癌,血液和骨髓里都可能有癌細胞存在,它們處于“休眠”狀態,日后一旦“蘇醒”,就擴散轉移;(2)癌細胞有兩類,一是普通癌細胞,二是癌干細胞。迄今化療和放療對癌干細胞均無能為力。這種癌干細胞便成為癌復發的種子。
對于肝細胞癌患者,有效治療后,應爭取去除病因。乙型肝炎感染者,應長期應用抗病毒藥物;丙型肝炎患者,應用干擾素類藥物控制病毒和肝內炎癥。
除此之外,應強調保持正確生活行為,盡可能消除或減少環境致癌因素,這里主要強調以下3點:
第一,消除慢性炎癥。如果將癌腫比喻為“火”的話,炎癥就是維持“火”燃燒“油”。炎癥能啟動和維持癌生長。相反地,控制炎癥能減少癌癥進展的危險。女性長期服用非甾體類固醇(NSAIDs)如阿司匹林或布洛芬,與沒有服用這些藥物的婦女相比,乳腺癌發生率明顯降低。
第二,消除自由基。可以把自由基比喻為風,給癌“火”煽風點火的“風”。 自由基也叫游離基,是氧化的產物。我們吸入的氧氣和吃進的食物,在氧化過程中會產生自由基;癌細胞本身能產生大量自由基,其生成速率遠高于正常細胞;腫瘤內常有免疫細胞浸潤,這些細胞也能產生自由基;化療藥之所以能破壞癌細胞,就是通過它產生的自由基。
第三,維護人體的免疫功能。免疫對癌細胞有監管、維持平衡的作用。我們可以免疫比喻為“墻”,阻止癌細胞擴散,至少與癌細胞維持“不戰不和”“和平共處”。為了達到消除慢性炎癥、消除自由基和維護免疫功能的目的,我們應保持良好生活行為,戒除可促進炎癥和自由基生成的生活習慣、方式。
忌什么?
對于可以促進氧化和慢性炎癥的因素,應盡可能避免或減少接觸。注意以下若干點:
• 戒煙:吸煙可加速高毒性或致突變自由基生成,促進炎癥性細胞活性,刺激已存在癌腫的生長。吸入二手煙同樣有害。
• 忌酒:大量飲酒,尤其飲烈性酒,可增加體內氧化應激,促進抗氧化劑轉化為促氧化劑,增加自由基生成,并能改變調節炎癥反應的酶活性,進而促進體內炎癥水平。但紅酒例外,它是強有力抗氧化劑。
• 避免肥胖:肥胖者患癌的機會增加。體內脂肪組織是白介素-6的主要來源,而白介素-6是促進慢性炎癥的細胞因子。超重的人血液中炎癥性因子水平升高。肥胖者體內胰島素和胰島素樣生長因子水平升高,這兩種物質均能促進癌細胞生長。
• 足夠睡眠:每天睡眠時間少于6小時者血液內白介素-6和α腫瘤壞死因子升高,兩者都是促進炎癥的因子。
• 減少暴露污染:污染可加劇炎癥,其機制包括氧化應激、破壞肝臟解毒功能、促發過敏反應,以及促進致炎癥性因子如α腫瘤壞死因子生成。已知接觸柴油、臭氧、汞以及煤燃燒的煙霧等可促進慢性炎癥。我們生活在充滿化學物的世界,空氣、水和土壤,無不被化學物污染,要完全避免這些化學劑是不可能的,但盡可能減少污染對自己的影響是可能的,例如在日常生活中,應避免家用化學清潔劑和房屋裝修造成的污染。
• 避免放射暴露:放射線和日光均可誘導自由基生成。
• 適當的健身:強烈的運動是不可取的,因為肌肉過度伸展可釋放炎癥因子,促進炎癥,促進自由基生成。理想的健身是每天或隔日一次做適度的肢體運動,以次日晨起不疲勞為度。運動應循序漸進,有節奏,持之以恒。
吃什么?
良好營養品有能力對抗現代生活中的各種疾病。對于康復期的癌癥病人,注意下列幾點:
• 少吃紅肉:過量攝食紅肉會促進結腸、肺、乳腺、食管、喉、胃、腎、子宮、卵巢和前列腺等器官的癌癥的發生。按1998年一項研究,每天進食一次紅肉、肝臟和腌肉的乳腺癌患者,復發率增加1倍,每天進食2次則使復發率增加4倍。
但應注意區別不同情況,例如在放化療期間,機體消耗很大,如沒有充足蛋白質供應,不利于受損的正常細胞和組織的修復。國外有專家建議多吃牛排,看來是有道理的。
• 葷素搭配,素食為主:素食主要指蔬菜(包括豆類)和水果。蔬菜和水果包含許多潛在有益的維生素、礦物質、纖維、胡蘿卜素,及其他生物活性物質,如黃酮類、萜類、甾醇、吲哚和酚類物質。不同顏色的蔬菜水果含有上述物質的量不盡相同。已有資料表明這些物質能降低肺癌、食道癌、胃癌和其他癌癥和大腸癌的風險。但不主張全素食。每人每天需蛋白質1.5-2.0克/公斤體重,如果體重60公斤,每天需蛋白質90-120克,癌癥病人消耗大,需要的蛋白質還要多,僅靠素食的供應是不夠的。雞蛋、魚和白肉富含優質蛋白質,不可不食。植物食物應多吃菌菇類,如蘑菇、香菇、平菇、猴頭菇、白木耳、黑木耳、鳳尾菇等,這些食物均含有豐富蛋白質。
• 適量食用牛奶和奶制品:關于癌癥患者飲奶是否有害?看法不一致。奶制品含有豐富蛋白質,對維護患者體質,促進正常細胞的修復(放化療破壞正常細胞)有好處。但有人認為飲奶可促進癌癥復發,因此大量食用是不恰當的。
• 少食精制碳水化合物:與正常細胞相比,癌細胞嗜好糖,消耗糖的數量5-15倍于正常細胞。腫瘤增殖愈快,消耗糖愈多。葡萄糖可使癌細胞無節制生長。在2型糖尿病患者,進食高糖食物引起血液葡萄糖和胰島素水平均升高,而胰島素會促進癌細胞攝取糖,其本身又能促進癌細胞尤其是結腸癌和乳腺癌生長。
• 少食脂肪:高脂肪食物能損傷DNA,導致癌細胞突變,逃逸放化療的作用,從而促進癌癥進展。高脂肪還能減低人體免疫功能,促進炎癥、血管新生,提高體內腫瘤生長促進因子水平。這可以解釋進食標準美國飲食的人發生癌癥的機會,超過以低脂、蔬菜為傳統食物的日本人和地中海地區人。
• 選食合適的脂肪:加氫油主要在工廠加工制成。部分加氫油能促進結腸癌進展。有資料顯示,食用含高加氫脂肪的結腸癌患者的抑癌基因(P53)發生突變的機會增加2倍。許多快餐食品常常用加氫油制成,因此應少食這些食品。
飽和脂肪:雖然是天然的,但也不是適宜的食品原料。由肉和乳提取的飽和脂肪能抑制人體免疫功能,降低機體解毒能力,增加氧化水平,促進自由基生成。
不飽和脂肪:比較有益于健康,其中Ω(奧米伽)3和9脂肪酸最有益,奧米伽6s作用最小。已知奧米伽3s能逆轉癌癥轉移,減少癌細胞對放化療的抵抗,增加某些化療藥的療效而減少其副作用。奧米伽9脂肪酸有明顯抗癌作用,在乳腺癌時,它能抑制乳腺癌基因HER2/neu,提高標靶藥赫賽停的療效。
對于癌癥病人,奧米伽3與奧米伽6的比例應是1:1到1:2。魚既能提供蛋白質,又能提供豐富奧米伽3s脂肪酸。其他含有豐富奧米伽3s脂肪酸的食物尚有菜油、核桃、亞麻仁、胡桃、各種果仁、芝麻、某些多葉綠色植物、許多藻類和海產植物等。雞蛋能提供奧米伽3,但應確定你吃的雞蛋來自奧米伽3脂肪酸喂養的雞。奧米伽9脂肪酸主要含于橄欖油、菜油、杏仁中,奧米伽6脂肪酸含于谷粒油和動物脂肪中。
• 選食具有抗炎癥作用的食物:可檢測體內炎癥水平,包括如C-反應蛋白、纖維蛋白原、前列腺素E2、血沉等,如果升高,說明體內有慢性炎癥存在,可選擇下列食物:①富含水楊酸的食物:天然抗炎癥成分存在于許多植物中,如鹿蹄草、姜黃和番茄。在有機食物、沒有接受殺蟲劑的食物中,水楊酸含量也很豐富;②富含類黃酮的蔬菜和水果。類黃酮不僅是強大的抗氧化劑,還能抑制COX2分子和在炎癥網中起關鍵作用的細胞因子。許多有顏色的植物均含有類黃酮,例如櫻桃含有最豐富的類黃酮,其次是新鮮的藍草莓、黑草莓等。類黃酮櫟精存在于洋蔥和蘋果中,已證明其能減少炎癥性TNF-α和白介素-8水平。
每天應選用至少2-4種以下富含抗炎癥成分的蔬菜:洋薊、花椰菜、黃瓜、洋蔥、西芹、菠菜、甜薯、番茄和南瓜。
在水果中,應選用以下水果中3-4種,包括蘋果、杏、黑草莓、藍草莓、甜瓜、櫻桃、越橘、西梅脯、木莓、紅葡萄、酸櫻桃等。
還有許多植物含有豐富的抗炎癥性因子,其中許多作為中藥在臨床上應用,包括月桂葉、辣椒、生姜、姜黃、芥末、肉豆蔻、牛至、迷跌香等。
• 選食具有抗氧化作用的食物:許多具有抗炎癥作用的食物也有抗氧化能力,例如牛至的抗氧化能力是蘋果的40倍,是橘子的10倍,藍莓的4倍。小茴香、新鮮大蒜、生姜、迷迭香、小鱗莖、孜然芹果和紅辣椒等,也含有豐富抗氧化劑;應多食有機食物;多食具有抗氧化作用的谷類,如大麥、小米、燕麥等;選食具有抗氧化能力的蛋白質:鮭魚中含有類胡蘿卜素抗氧化劑;豆制品如豆腐、豆奶,以及其他植物如花豆、黑豆、蠶豆、四季豆和小紅豆等,均含有豐富的抗氧化劑,應每天或隔天食用。
• 適當的食品加工。避免長時間和高溫烹飪。碳水化合物和蛋白質經深度油炸和炭烤后,產生一種糖毒素,這是一種高度致炎癥性物質。因此食物烹飪時宜采用相對低溫的蒸煮方法。
研究表明,食物中許多成分對癌癥復發具有預防作用,這些成分有硫代葡萄糖苷、類黃素、維生素A/D/E、硒、姜黃素、類胡蘿卜素等,每一種成分相對地對某一種或幾種癌癥有預防作用。這些成含于多種蔬菜和魚類中。
• 在各種食物抗癌成分中,植物色素具有特殊作用,其中最著名的是番茄紅素,見于番茄和許多紅色蔬菜如西爪、葡萄和柚子中,是抗氧化劑類胡蘿卜素的一種,能抑制前列腺癌。
• 在眾多含有抗癌活性成分的蔬菜中,十字花科蔬菜防癌、抗癌能力最強。蘿卜硫素,又稱“萊菔硫素”,在西蘭花、芥藍和甘藍等十字花科植物中含量較豐富,具有抗氧化作用,對胰腺癌、結腸癌、乳腺癌、肺癌和前列腺癌等有良好的抗癌活性。現認為,蘿卜硫素是蔬菜中所發現的抗癌效果最好的植物活性物質。十字花科蔬菜還含有吲哚-3-甲醇,能阻止癌腫轉移,并能改變雌激素代謝,減少其對乳腺癌的促進作用。十字花科蔬菜還含有2-苯基乙基異硫代氰酸酯,該物質能引起癌細胞自殺。
• 草莓中紫紅色素叫花青素,與番茄紅素一樣,也具有抗氧化作用。接木草莓中花青素能被血管內皮細胞攝取,防止自由基作用于這些細胞發生突變。山莓中含有鞣花酸,在體外實驗中能抑制乳腺癌和宮頸癌細胞生長。草莓中還含有一種化學物質能血管內皮生長因子活性,引起癌細胞缺血缺氧。槲皮素存在于色彩鮮艷的蔬菜和水果,如蘋果、羽衣甘藍和紅蔥中,能是耐化療藥的乳腺癌細胞恢復敏感性。
• 茶能增強體質,其含有的多酚具有抗氧化、抗病毒、抗炎癥活性,能調節解毒酶,刺激免疫功能,減少血小板凝聚。在多酚中,表沒食子兒茶酚對健康最有促進作用。綠茶優于黑茶。綠茶已被證明有預防癌癥的作用,能誘導腫瘤抑制基因,抑制導致DNA受傷的基因表達,阻抑許多實驗性腫瘤生成和擴散。
• 咖啡對結腸癌有預防作用。哈佛大學曾對5272例乳腺癌患者做了調查,發現飲含咖啡因飲料的絕經期婦女患乳腺癌的危險性降低。哈佛大學的另一組學者調查了皮膚癌與咖啡的關系,每天飲咖啡多于3杯者發生基底細胞癌的危險性明顯低于每天飲咖啡少于1杯的人。
“補”什么?
市場上“防癌抗癌”的“補藥”“營養品”琳瑯滿目,真假難分。在選擇時,應考慮①原料是什么?②哪些成分?③什么工藝?④有無添加劑?如從抗氧化和抗自由基角度考慮,可以應用維生素C/E、葡萄籽浸出物、胡蘿卜素等。
應聯合應用幾種或多種抗氧化劑。生育酚即維生素E應聯合應用α和γ型,同時配上維生素C和α脂酸。另外還需要考慮患者的疾病和病史,例如肺癌,尤其在以前或現在吸煙者,應避免給予大劑量單個抗氧化劑,尤其維生素E、β胡蘿卜素和維生素A,因為煙草可將這些抗氧化劑變成危險的促氧化劑,引起相反的后果。
為了消除炎癥,可應用維生素E、姜根或姜黃根制劑等,它們針對不同的炎癥性分子。
也可按試驗選擇“補品”。根據試驗異常情況,選擇不同的營養制劑。一般應堅持使用這些制劑3個月,如果試驗結果恢復正常,可長期應用多種維生素、魚油、綠色蔬菜和水果以維持效果。
怎樣運動?
有效治療后應保持運動,對于預防復發有益。這是因為:
• 生長刺激性激類包括雌激素、胰島素和胰島素樣生長因子能促進乳腺癌、前列腺癌和其他實質性腫瘤發生,運動能減少這些激素的水平;運動還能減少胰島素抵抗,減低體內胰島素水平;
• 氧化應激會產生自由基,后者是反應性分子,促進癌癥發生。運動可刺激一種酶生成,消除這些自由基;
• 運動可增強免疫系統尤其是自然殺傷細胞(NK)的生成和活力,阻止癌細胞轉移。運動能促進肌肉釋放谷氨醯胺,后者能刺激NK細胞;
• 炎癥能促進癌發展,運動可增加抗炎癥性分子活性,從而減緩癌癥發展;
• 運動能調節患者心情,促進睡眠,減少憂慮和抑郁。有認為運動能直接升高腦內一種物質的水平,減少憂郁;
• 運動能促進血液循環,改善組織的氧和營養物供應,而癌癥在有氧狀態下進展減慢;
• 運動可減低血液粘稠度,減少血小板凝聚,從而減少癌癥時常常發生的血栓形成;
• 運動能改善消化功能,促進營養物尤其是微量元素的吸收;
• 運動可促進腸蠕動,減少腸內容通過時間,減少或防止便秘發生。
運動的方式和程度因人而異。運動量應適宜。前已述及,過激、過猛的運動可促使自由基生成。鍛煉后身體感到發熱,輕微出汗,無疲勞感,身心感到輕松、舒暢,食欲和睡眠良好,說明運動恰當。否則,則應調節運動量,使身心處于最佳狀態,以利于康復。
郭林氣功看來是一種剛柔適當的特殊運動,它將“有氧呼吸”和肢體運動結合起來。美國已將郭林氣功列為“整合療法”之一。