近日,“國家呼吸系統疾病臨床醫學研究中心-中國呼吸腫瘤協作組大會2021年會暨第三屆粵港澳大灣區呼吸腫瘤診治新進展學習班”在廣州隆重舉行。本次會議多位國內腫瘤界名醫齊聚一堂,旨在加強粵港澳大灣區呼吸腫瘤學術領域的交流與合作,促進肺癌診治技術水平的持續發展。我院牛立志院長應邀出席大會并作主題發言,展示并分享了康博刀在肺部領域的應用、研究的進展、患者的治療情況以及臨床中所積累的經驗,在此大會上與國內同道共商肺癌診療當前的難題和未來的發展方向。


會議現場
肺癌是常見的惡性腫瘤之一,是我國發病人數和死亡人數最多的癌癥,嚴重危害著我國人民的健康與生命。由于早期癥狀不明顯,部分處于中晚期的患者在確診時已喪失手術機會。微創消融手術治療在肺部領域已取得顯著療效,為中晚期不能和不愿意接受外科切除的肺癌患者提供了新的治療機會。
何時該采用熱消融?
何時該采用冷消融?
牛立志院長表示,對于直徑≤3cm的腫瘤,射頻消融、微波消融、冷凍消融這三種消融方式均可獲得良好的治療效果。射頻消融電極的適形性好,可以通過調節消融電極來保護鄰近臟器,但是受血流和氣流的影響較大;
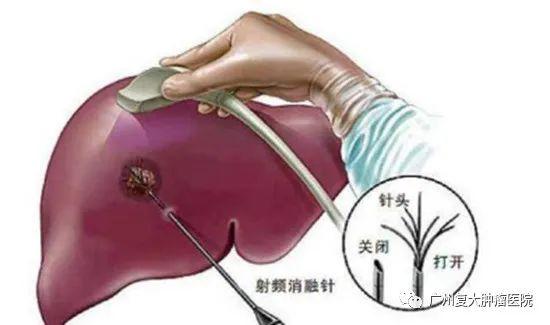
對于直徑>3cm,尤其是>5cm的腫瘤,微波消融因其消融時間短、消融范圍大,明顯優于其他兩種消融方式,且微波消融受到血流灌注的影響小,更加適合治療鄰近大血管的腫瘤。
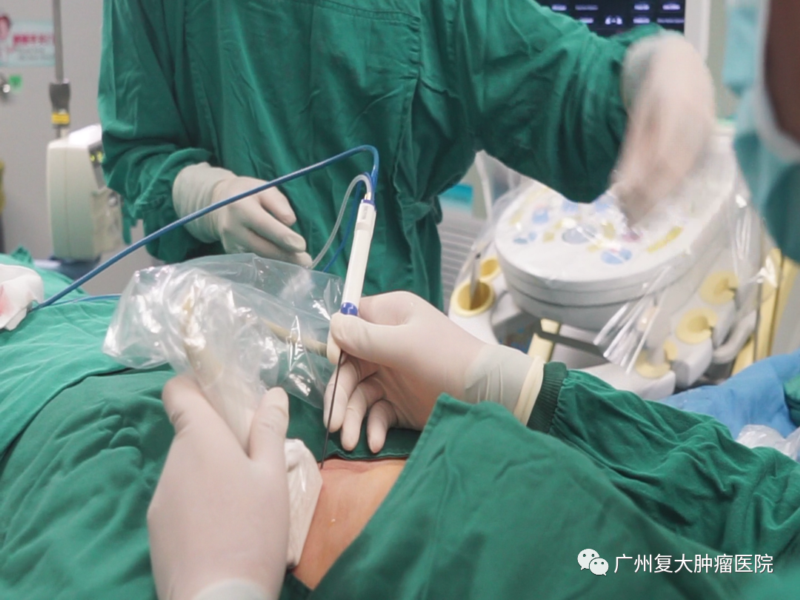
冷凍消融形成的“冰球”邊界清晰,易于監測,可用于鄰近重要臟器的肺部腫瘤。冷凍消融較少引起局部疼痛,更適用于腫瘤距離胸膜≤1 cm或有骨轉移引起骨質破壞的腫瘤患者。但冷凍消融在治療過程中消耗患者血小板,對于凝血功能差的患者,應避免使用冷凍消融。
單一的冷凍或加熱治療均存在一定的局限性,而康博刀作為一種復合式冷凍消融設備,屬于第四代冷凍消融技術。它既包含傳統冷凍耐受性好、安全性高、無需全身麻醉、可影像監測,可用于大血管、心臟附近腫瘤,可用于起搏器植入患者,可激發免疫等優勢,又克服了傳統的氬氦刀冷凍消融易出血、存在針道種植風險及熱消融病人疼痛明顯、耐受差等問題。
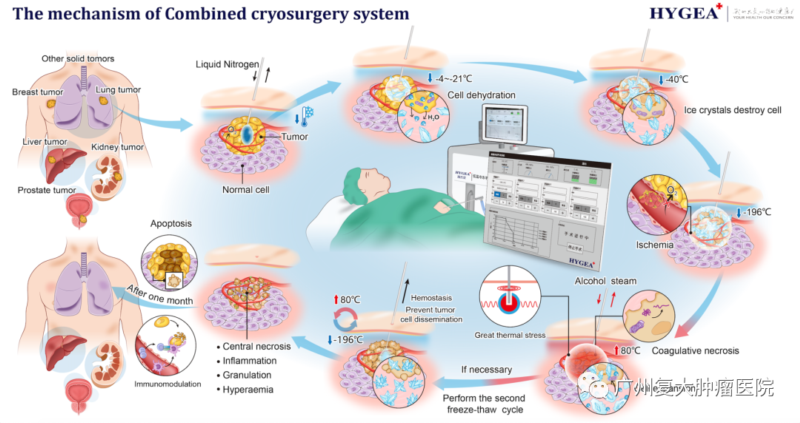
患者吳先生因異常凝血酶原明顯升高,做了全身PET/CT發現雙肺有小結節,大小約1.61mm×15.1mm和9.5mm×7.9mm。由于害怕加上同時治療兩個肺結節會更容易產生氣胸,吳先生在醫生的建議下于當地醫院做了右肺占位射頻消融術。
術后結節雖有好轉,但他出現了右肺消融處出現感染發燒。為求進一步診斷,吳先生來我院就診。其CT平掃+三維重建顯示他右肺有局部空洞形成并與支氣管相通;左肺上葉前段可見一大小約8×7mm小結節狀密度增高影,邊界不清。
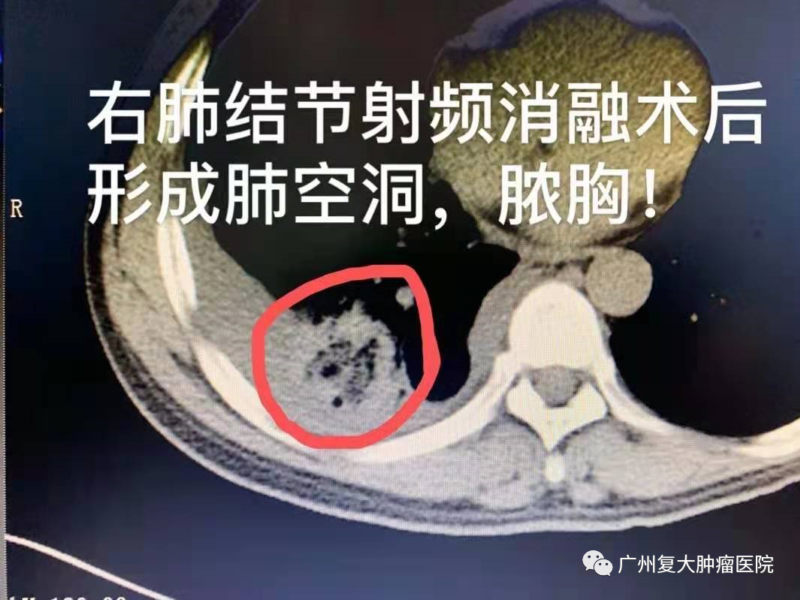
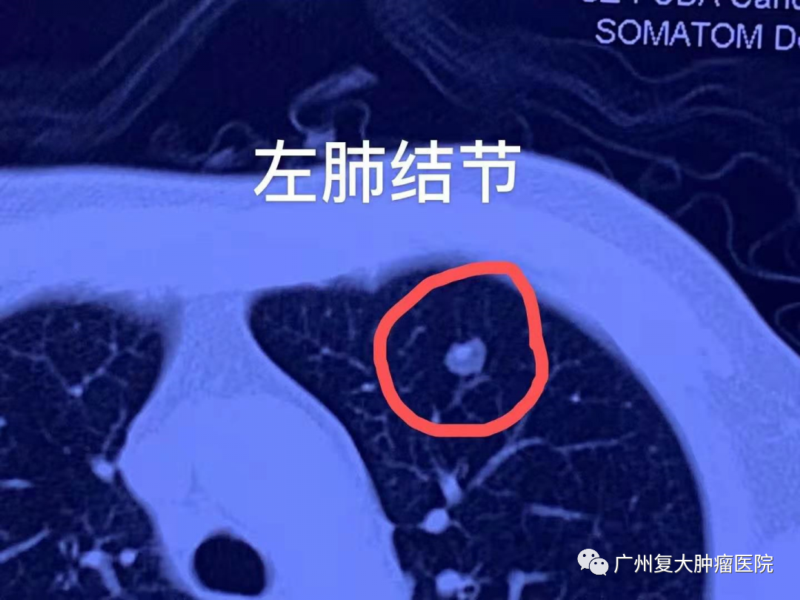
吳先生在接受抗感染治療控制發燒癥狀、改善右側氣胸以及胸腔積液的問題后,牛立志院長為吳先生做了左肺結節康博刀冷凍消融術,術程順利。
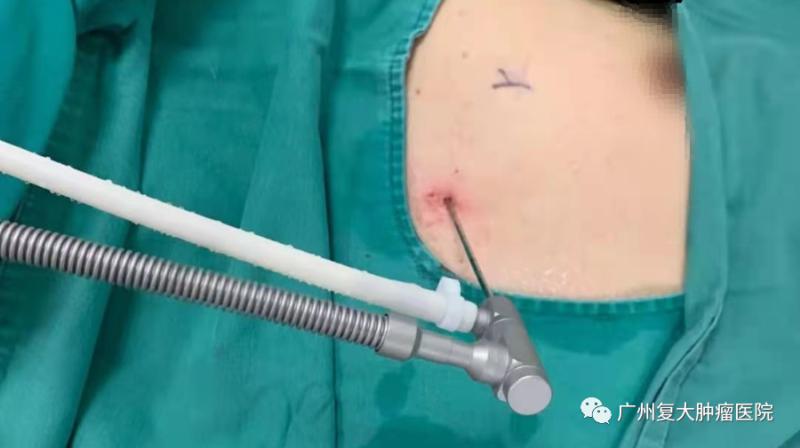
冷凍消融治療
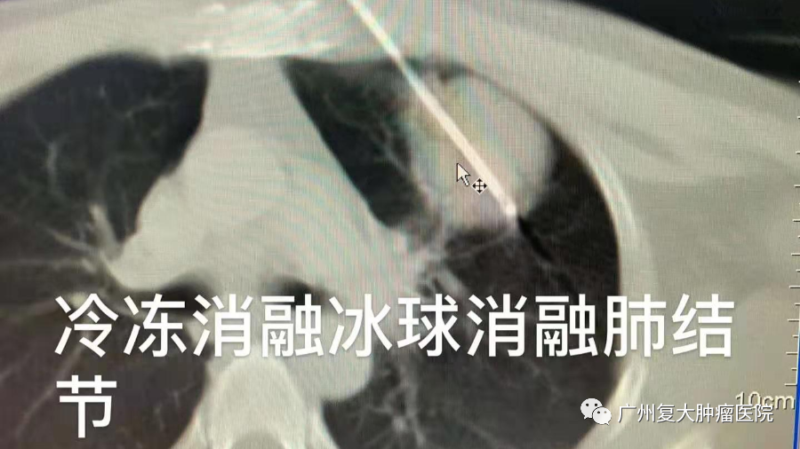
牛立志院長介紹,在靠近胸壁的情況下,康博刀冷凍消融治療引起的機體疼痛刺激比較小,在凍死腫瘤的同時,不會像射頻消融一樣,容易形成“肺空洞”。
近兩年康博刀已廣泛應用于肺癌、肝癌、乳腺癌、前列腺癌、腎癌、骨癌及腹腔腫瘤、軟組織腫瘤等多種實體腫瘤,其治療效果已得到國內外臨床界廣泛認可。它具有以下優勢:
第一,技術層面:這種集深低溫冷凍和高強度加熱于一體的復合式腫瘤消融治療技術方案,結合了冷凍消融和熱消融的優勢作用,摒棄了單一功能治療設備的缺陷,殺傷腫瘤更徹底,高溫加熱可大幅減少針道出血,實現了更好的安全有效性;
第二,主機方面:通過深低溫與高溫精確協同流動控制,實現多通道均勻平穩運輸,同時對運輸路徑的優化設計,實現了高強度冷熱獨立快速切換,解決了國內外液氮冷凍系統“冷堵”的難題;
第三,消融針方面:在微細消融針中實現了整體極低漏熱和局部高強度換熱。通過將一根直徑約2mm的消融探針經皮穿刺進入腫瘤靶向部位,對病變組織交替實施深度冷凍(低溫-196℃)和加熱(80℃以上)的物理刺激,實現了治療溫差跨越;

第四,在耗材與設備層面:康博刀使用液氮等極易獲取的耗材,降低成本,工作時低壓運行,安全可靠。
近年來腫瘤治療逐漸向微創化、精準化轉變。以腫瘤消融治療為代表的微創技術以“降低損傷人體結構、有效殺滅腫瘤”為原則,具有創傷小、減少疼痛、療效突出、激發免疫等優勢,在肺部領域尤其是多發肺結節、晚期肺癌等發揮重要作用。而冷凍消融技術與現代影像學技術、靶向藥治療、免疫治療等有機結合也逐漸成為未來發展趨勢。